Апластическая анемия
Содержание:
Причины возникновения апластической анемии
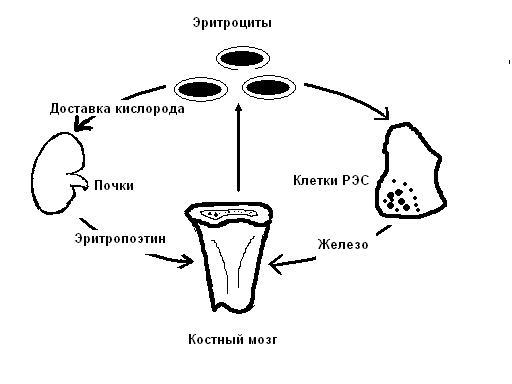
Апластическая анемия — это гематологический синдром, обусловленный действием большого количества экзогенных и эндогенных факторов. Характерным его признаком являются качественные и количественные изменения клеток гемопоэза и их микроокружения с развитием панцитопении в периферической крови, гипоклеточности и жировой инфильтрации костного мозга.
Определяют два возрастных пика заболеваемости апластической анемией — 20 и 65 лет. В связи с этим существует мнение о возможной этиологической роли вирусов (в молодом возрасте) и химических веществ (в пожилом). Однако большинство авторов склонны считать апластическую анемию полиэтиологическим заболеванием.
Вероятную причину возникновения апластической анемии выявляют примерно у 50% больных. К возможным этиологическим факторам относятся:
- некоторые лекарственные препараты (антибиотики, сульфаниламидные препараты, препараты золота, нестероидные противовоспалительные и успокаивающие средства, транквилизаторы, цитостатики и т.п.),
- химические вещества (пары ртути, кислот, красители, лаки, краски, средства бытовой химии, бензин, бензол, урсол и т.п.),
- физические факторы (радионуклиды),
- инфекционные агенты (вирусы гепатитов В, С, ретровирусы, микобактерия туберкулеза и т.д.),
- аутоиммунные процессы и заболевания (системная красная волчанка, синдром Шегрена, эозинофильный фасциит и т.п.).
В развитии апластической анемии имеет значение генетическая предрасположенность и индивидуальная реактивность организма. Рассматривают три главные концепции возможных механизмов возникновения нарушений костномозгового кроветворения при апластической анемии:
- поражение стволовых кроветворных клеток,
- нарушение иммунологического контроля за процессами гемопоэза (клеточного и гуморального),
- дефектность кроветворения микроокружения.
Первые клинические проявления апластической анемии бывают различными. Острое начало наблюдается в 12-15% больных. Для него характерны быстрое развитие анемии, выраженный геморрагический синдром, часто — лихорадка с ознобом. Острое начало обычно наблюдают с молодых людей. Чаще апластическая анемия развивается постепенно, проявляется анемичным и геморрагическим синдромами. Ход определяют у 85% больных апластической анемией.
Поводом для первичного обращения к врачу может быть нарастающая общая слабость, вялость, бледность, появление одышки и сердцебиения при ходьбе, боли в области сердца как признак анемической гипоксии. Иногда наблюдаются геморрагические проявления различной степени и локализации — кровотечения носовые и с десен, кожные геморрагии (от мелкоточечных до сплошных), меноррагия. Нередко возникают гематурия, кровотечения из пищеварительного тракта.
В 84% больных во время офтальмоскопии обнаруживают кровоизлияния в сетчатку. Часто наблюдают горячку, обусловленную некротическими изменениями слизистых оболочек ротовой полости, пищеварительного тракта, нагноением обширных кровоизлияний во внутренних органах и тканях. Таким образом, клинические проявления апластической анемии непосредственно связаны с изменениями в периферической крови (анемия, лейкопения, тромбоцитопения) и охватывают соответственно тощий, геморрагический синдромы и синдром инфекционных осложнений.
Для апластической анемии не характерны спленомегалия, гепатомегалия, увеличение лимфатических узлов. Увеличение размеров печени можно наблюдать разве что у лиц, переболевших гепатитом, а селезенки — у пациентов, которым неоднократно проводили гемотрансфузии. Апластическая анемия чаще развивается в течение длительного времени (месяцы и годы), может сопровождаться сначала редукцией одного из ростков кроветворения с постепенными изменениями со стороны всех ростков.
Апластическая анемия – причины
Выделить единственную причину невозможно, так как вызвать апластическую анемию могут различные факторы. Они разительно отличаются друг от друга, но могут приводить к одинаково тяжелым последствиям.
Справочно. Выделяют два основных типа заболевания – врожденный и приобретенный. В первом случае ребенок первоначально содержит генную мутацию, которая приводит к нарушению кроветворной функции. Во втором варианте нарушение выработки клеток крови происходят под влиянием внутренних (эндогенных) или внешних (экзогенных) факторов.
Клиническая картина этих вариантов отличается. Во-первых, врожденные формы часто проявляются на ранних сроках жизни. Во-вторых, они могут сочетаться с аномалиями развития различных органов.
Внимание. В зависимости от вида хромосомной мутации, может наблюдаться снижение производства лишь одного вида кровяных клеток.. При манифестации во взрослом возрасте первыми симптомами могут быть общее недомогание и головокружение, которые являются неспецифичным и возникают при многих заболеваниях
Скорость прогрессирования апластической анемии зависит от выраженности нарушения кроветворной функции
При манифестации во взрослом возрасте первыми симптомами могут быть общее недомогание и головокружение, которые являются неспецифичным и возникают при многих заболеваниях. Скорость прогрессирования апластической анемии зависит от выраженности нарушения кроветворной функции.
Апластическая анемия у детей (врожденная)
Врожденные формы включают в себя следующие варианты: 
- Синдром Даймонда-Блекфена. При данной патологии происходит нарушение на уровне клеток-предшественников эритроцитов. Фенотипическим симптомом является бледная кожа. Увеличение печени и селезенки не характерно, но может развиваться с течением времени.
- Анемия Фанкони. Наследственное заболевание, которое проявляется на пятом десятке жизни. Возникает острый лейкоз и апластическая анемия. Для данной генной мутации характерны аномалии развития, которые проявляются уже на ранних сроках жизни. В основном это аномалии костной системы (низкий рост, маленький череп, недоразвитие первого пальца верхних конечностей, лучевой кости, тяжелая дисплазия бедра, дополнительное ребро) и неврологический дефицит (аномалии глазных яблок, косоглазие, птоз, нарушение слуха, умственные нарушения развития).
- Синдром Эстрена-Дамешека. Помимо нарушения кроветворения для данных детей характерна определенная внешность – светлые волосы, широко расставленные глаза, курносый нос. Апластическую анемию в этом варианте сопровождает увеличение печени и селезенки.
Приобретенная апластическая анемия
Приобретенные формы различают по факторам, которые вызывают апластическую анемию.
- Внешние (экзогенные) факторы:
- Медикаментозное влияние – прием сульфаниламидов, антибактериальных средств (тетрациклин, левомицитин, стрептомицин), средств для лечения туберкулеза (изониазид, ПАСК), анальгина, цитостатиков.
- Воздействие химических агентов – наиболее опасны нефтепродукты, бензольные производные, ртуть.
- Радиоактивное воздействие.
- Инфекции. Наиболее опасными являются вирус, вызывающий гепатит С, цитомегаловирус, герпес-вирус. Чаще всего они оказывают выраженное повреждающее действие лишь при активно перенесенном заболевании.
- Внутренние (эндогенные) факторы:
- Аутоиммунное поражение костного мозга. Чаще наблюдается в пожилом возрасте.
- Эндокринное влияние. Выявлена связь с нарушением функции щитовидной железы, и с заболеваниями яичников у женщин.
Внимание. Данное разделение условное, так как даже экзогенные факторы могут влиять на костный мозг опосредованно через запуск аутоиммунной агрессии.
Причины и симптомы
Медицина до сих пор не имеет однозначного ответа на то, какие конкретные причины апластической анемии. Однако есть факторы, принимающие участие в формировании болезни:
- контактирование с веществами, имеющими повышенную активность;
- применение некоторых классов лекарственных средств;
- выделяют также инфекционные провокаторы болезни;
- генетические предпосылки;
- облучение также способно спровоцировать апластическую анемию.
Среди специалистов бытует мнение, что беременность способна повышать апластические изменения в костном мозге, тем не менее, патогенетического обоснования этой теории нет. Обнаружение признаков болезни во время беременности является показателем к её прерыванию. Зарегистрированы случаи, когда болезнь переходила в стадию ремиссии после искусственных родов.
К причинам следует также отнести аутоиммунные патологии, в процессе которых иммунные механизмы, кроме того, что ведут борьбу с болезнетворными агентами, так ещё и наносят вред собственным клеткам костной ткани.
Если причину болезни не удаётся установить, ставится диагноз идиопатическая апластическая анемия.
Иногда заболевание очень остро начинается и молниеносно прогрессирует. Но, в большинстве случаев возникновение болезни начинается долго и постепенно, на протяжении длительного времени больные могут не догадываться о ее течении, списывая незначительные симптомы на общее недомогание организма.
Симптомами апластической анемии являются любые признаки недостатка клеток в крови:
- при недостатке эритроцитов наблюдается слабость, бледность кожного покрова на лице, частые головокружение, периодические шумы в ушах, беспричинная одышка;
- если не хватает тромбоцитов, во время малейшего контакта кожи с любыми предметами возникают синяки, также отмечается кровоточивость из десен и носа;
- если же в крови не хватает лейкоцитов, тогда организм сигнализирует об этом частыми мочеполовыми инфекциями, ангиной, пневмонией.
Уже первый осмотр пациента может дать чёткую картину заболевания: бледность, синюшность кожи, сопровождаемая кровоподтеками без четких границ. Появление отёчности в ногах и увеличение размеров печени говорят о выраженной сердечной недостаточности. Главным признаком, который помогает установить апластическую анемию, являются неизменные размеры селезёнки.
Тяжесть проявления симптомов напрямую зависит от того, какая степень угнетения ростков кроветворения.
Диагностика Апластической анемии:
Анемия выражена очень сильно, иногда гемоглобин снижается до 20-30 г/л. Анемия чаще нормохромная, макроцитарная. Содержание ретикулоцитов колеблется от 0 до 4-5%. Тяжелые формы сопровождаются большим снижением уровня ретикулоцитов. Эритрокариоциты в периферической крови появляются редко. Отмечается выраженная гранулоцитопения. Иногда количество гранулоцитов снижается до 0,2 Ч 109/л, при этом развиваются инфекционные осложнения. Иногда снижается абсолютное количество моноцитов. Абсолютный уровень лимфоцитов в большинстве случаев остается нормальным. Снижается количество тромбоцитов, при этом значительно удлиняется время кровотечения и, как следствие, развивается геморрагический синдром, СОЭ ускоряется до 30-50 мм/ч.
Количество миелокариоцитов костного мозга заметно снижается. Иногда отмечается раздражение красного ростка. Увеличено количество лимфоцитов, плазматических, тучных клеток. Мегакариоциты могут полностью отсутствовать. В костном мозге резко увеличивается количество железа, расположенного как в эритрокариоцитах, так и внеклеточно.
Содержание железа сыворотки у большинства больных увеличено, насыщение трансферрина приближается к 100%. При исследовании феррокинетики при помощи радиоактивного железа выявляются удлинение времени выведения железа из плазмы и снижение количества железа, включенного в эритроциты. Продолжительность жизни эритроцитов, измеренная при помощи радиоактивного хрома, чаще всего укорочена, реже – нормальная. Иногда повышается уровень фетального гемоглобина. Агрегатгемагглютинационная проба часто оказывается положительной. На поверхности эритроцитов выявляют IgG. Необходимо исключить присутствие аллоантител на поверхности недавно перелитых эритроцитов.
Диагностика апластической анемии возможна только после гистологического исследования костного мозга. Выявление панцитопении в периферической крови служит показанием к стернальной пункции (костномозговая пункция, производимая через переднюю стенку грудины) для исключения гемобластоза и витамин-В12-дефицитной анемии. После этого производится исследование взятого материала. При выявлении большого количества жира в костном мозге диагностируют апластическую анемию. Если при исследовании обнаруживается нормальное соотношение между кроветворной тканью и жиром или имеется структурное увеличение клеток, то диагноз апластической анемии отпадает. При этом нередко увеличивается селезенка, иногда бывает положительная проба Кумбса, но чаще антитела обнаруживаются при помощи агрегатгемагглютинационной пробы. В костном мозге — нормальное количество мегакариоцитов, тогда как при апластической анемии мегакариоциты почти полностью отсутствуют. При периферической панцитопении у пожилых людей, у лиц с удалением части желудка следует в первую очередь исключить витамин-В12-дефицитную анемию, у детей -фолиеводефицитную анемию.
Апластическая анемия у детей
В детском возрасте чаще дебютируют врожденные типы апластических анемий, к которым относятся анемии Фанкони и Блекфена-Даймонда.
Анемия Фанкони представляет собой наследственную патологию, наследуемую по аутосомно-рецессивному типу, то есть случаи заболевания наблюдаются только в семьях, где оба родителя являются носителями патологического гена. Проявляется анемия Фанкони не только в глубоком угнетении всех типов кроветворения, но и в появлении аномалий развития.
Дебют заболевания приходится на возраст 4-12 лет, но гематологические проблемы могут возникнуть непосредственно после рождения ребенка. К врожденным аномалиям относятся: несоответствие костного возраста паспортному, врожденные пороки сердечно-сосудистой системы, микроцефалия, аномалии развития костной ткани, органов мочеполовой системы, отставание в психомоторном развитии. Гематологические изменения проявляются в более позднем возрасте (в среднем по достижению 9 лет) и в клинической картине преобладают симптомы геморрагического симптомокомплекса, после чего прогрессивно нарастают признаки лейкоцитопении и эритроцитопении.
Данная патология имеет стремительное прогрессирующее течение, поэтому при отсутствии адекватного лечения летальный исход наступает в течение 6 месяцев. Причиной смерти чаще всего является массивное желудочно-кишечное кровотечение или мозговое кровоизлияние. Осложнениями анемии Фанкони является трансформация заболевания в острый лейкоз, а также онкопатология органов желудочно-кишечного тракта. Единственным эффективным методом лечения врожденной анемии Фанкони является трансплантация костного мозга.
Анемия Блекфена-Даймонда относится к группе спорадических наследственных патологий крови и характеризуется поражением исключительно эритроцитарного ростка кроветворения. Дебют заболевания наблюдается в течение первого года жизни ребенка.
Дети с анемией Блекфена-Даймонда имеют типичный фенотип: бледные кожные покровы, крупная верхняя губа, широко поставленные глаза, сухие секущиеся волосы, отставание костного возраста от паспортного.
Характерным изменением лабораторных показателей периферической крови является прогрессирующая нормохромная анемия при полной сохранности пролиферации клеток тромбоцитарного и гранулоцитарного ряда.
Данная патология характеризуется вялотекущим хроническим течением со склонностью к спонтанной ремиссии. Предпочтительным методом лечения является применение кортикостероидной терапии, а также по жизненным показаниям переливание эритроцитарной массы.
В детском возрасте приобретенные формы апластической анемии встречаются крайне редко и проявляются теми же симптомами, что и у взрослых при полном отсутствии врожденных патологий.
При наличии у ребенка признаков нарушения кроветворной функции костного мозга обязательно необходимо проводить дифференциальную диагностику с такими заболеваниями как: острый лимфобластный и миелобластный лейкоз, мегалобластная анемия, синдром гиперспленизма, метастатическое поражение костного мозга.
Ребенок с подозрением на врожденную апластическую анемию обязательно подлежит комплексному обследованию, к которому относятся: цитогенетический анализ после трепанобиопсии, анализ крови на предмет наличия антител к клеткам крови, рентгенография с определением костного возраста, миелограмма. Также обследованию подлежат все ближайшие родственники больного ребенка.
Диагностика
Для установления диагноза пациенту требуется тщательное обследование и сдача определённых анализов. В частности, пациентам назначается:
- общий анализ крови, в котором можно увидеть снижение количества кровяных клеток;
- БАК (биохимия);
- анализ крови на ретикулоциты;
- пункция костного мозга для последующей оценки состояния всех ростков кроветворения;
- биопсия костного мозга для уточнения стадии заболевания и определения количества кровяных клеток в нём. При данной патологии определяется, что большая часть костного мозга заменена жировой тканью, из-за чего орган не может справляться с функцией кроветворения.
Апластическую анемию подозревают у пациентов с панцитопенией, особенно молодых. Тяжелая апластическая анемия определяется наличием 2 или более следующих признаков:
- Клеточность костного мозга < 30%
- Абсолютное количество нейтрофилов < 500/мкл
- Абсолютное количество ретикулоцитов < 60 000/мкл
- Количество тромбоцитов < 20 000/мкл
Возможно, диагностические мероприятия на этом не закончатся и для уточнения предварительного диагноза потребуются дополнительные тесты:
- Цитогенетический анализ КМ и лимфоцитов, циркулирующих на периферии, – для выявления хромосомных аберраций, если они есть;
- Ультразвуковое исследование (УЗИ) печени, селезенки, вилочковой железы (у детей, поскольку у взрослых она уже завершила свою деятельность), лимфатических узлов;
- Определение наличия вирусов в организме (Эпштейн-Барр, цитомегаловирус, маркеры гепатитов, ВИЧ, ВПГ и др.);
- Компьютерная томография – КТ (проводится с целью исключить вторичную гипоплазию КМ)
- Иммунологическое исследование (определение состояния иммунитета на клеточном и гуморальном уровнях);
- Типирование антигенов HLA II класса (ПЦР), если предполагается пересадка костного мозга.
Разумеется, перед тем как приступить к обследованию, врач тщательно собирает и изучает семейную историю, анамнез жизни и болезни пациента. Диагностические мероприятия, предусматривающие использование инструментальных методов (пункция КМ), а также проведение операций после установления диагноза (спленэктомия, пересадка костного мозга) требуют письменного согласия больного или его родителей (если подобные процедуры осуществляются у детей).
В случае диагностики апластической анемии у детей, важно определить, не является ли она наследственной формой – анемией Фанкони, так как лечение этого заболевания отличается от лечения классической формы патологии. Для определения формы проводятся цитогенетические исследования
Апластическая анемия – основные разновидности
Апластическая анемия, как заболевание, было открыто еще в 19 веке. Однако тенденция его развития абсолютно не радует. С каждым годом заболевших становится все больше. Радует лишь то, что апластическая анемия – это не всегда смертельный приговор. Развитие современной трансплантологии позволяет пересаживать костный мозг человеку и спасать ему жизнь. Также определенный вклад в лечение данного нарушения вносит схема лечения иммуносупрессорами.
Современная медицина выделяет 2 вида апластической анемии (приобретенную и врожденную/наследственную), которые, в свою очередь, разделяются на несколько подвидов. Каждый из них необходимо рассматривать отдельно.
Подвиды апластической анемии приобретенной формы:
Истинная анемия, которая в половине случаев является идиопатической, то есть причины ее возникновения установить невозможно. При истинной анемии происходит угнетение всех направлений системы кроветворения.
Варианты развития заболевания могут быть следующими:
Острая анемия продолжается не более 60 дней и всегда заканчивается летальным исходом.
Подострая форма болезни может длиться от 60 дней и более. Если речь идет об апластической анемии, то состояние больного может стабилизироваться, но на непродолжительный отрезок времени. При гипопластической анемии ремиссии могут быть более длительными, но они все равно будут сменяться острыми фазами.
Хроническая форма болезни. Течение анемии сглажено, летальный исход наступает спустя 3-5 лет от манифестации болезни, в редких случаях пациенты живут до 10 лет. Еще реже у больных наступает выздоровление.
Парциальная красноклеточная аплазия костного мозга (ПККА) – это приобретенная апластическая анемия, которая имеет аутоиммунную природу. Костный мозг не в состоянии выполнять свои привычные функции, так как на антигены его эритрокарцитов воздействуют аутоантитела, разрушая их. Чаще всего причину парциальной аплазии уточнить не удается. Хотя в ряде случаев заболевание может развиваться на фоне опухолевых новообразований вилочковой железы. В подростковом возрасте парциальная красноклеточная аплазия может заканчиваться выздоровлением больного. Поэтому специалисты выделяют эту патологию в отдельную форму, называя ее подростковой ПККА.
Гипопластическая анемия с гемолитическим компонентом. Многие ученые утверждают, что это разновидность заболевания является лишь стадией пароксизмальной ночной гемоглобинурии. Отличительной чертой этой разновидности болезни является то, что она периодически сопровождается гемолитическими кризами.
Кроме приобретенной апластической анемии, различают врожденную и наследственную форму болезни.
Они, в свою очередь, подразделяются на следующие виды:
Анемия Фанкони, которая передается по аутосомно-рецессивному типу. Проявляется у носителей гомозигот в период от 4 до 10 лет. Анемия Фанкони может сопровождаться грубыми изменениями в развитии внутренних органов, а может протекать с незначительными их повреждениями.
Анемия Джозефа-Даймонда-Блекфена. По какому типу наследуется эта патология до настоящего момента времени учеными не установлено. Имеются предположения, что передача дефективных генов происходит по аутосомно-доминантному типу, хотя другие ученые настаивают на аутосомно-рецессивном способе передачи. Единой точки зрения по этому вопросу нет. Патология манифестирует практически сразу после появления ребенка на свет. Как правило, к 4 месяцем у 2/3 детей уже имеются первые ее признаки. Если их нет, то они обязательно появятся к тому времени, когда ребенку исполнится год. Этот вид анемии может сопровождаться тяжелыми повреждениями внутренних органов, либо протекать без подобных изменений.
Гипопластическая анемия Эстрена-Дамешека. В этом случае у больного ребенка будут наблюдаться нарушения функции кроветворения, но аномалии развития не обнаруживаются.
Если гипопластическая анемия развивается на фоне врожденных аномалий развития, то заболевание манифестирует в раннем возрасте. При приобретенной форме болезни человек рождается абсолютно здоровым.
Течение и симптомы
Заболевание может протекать остро, подостро или хронически. В острых случаях процесс начинается с бурного геморрагического диатеза (см. Геморрагические диатезы), тяжелой общей интоксикации, инфекционных осложнений. Чаще наблюдается постепенное нарастание симптомов. Появляются адинамия, слабость, головокружение, быстрая утомляемость, одышка при физ. нагрузке, иногда боли в костях и области сердца. Отмечается восковидная бледность кожи без желтушности, малокровие видимых слизистых оболочек. Подкожная жировая клетчатка сохранена. При развитии глубокой тромбоцитопении (см.) возникают кровоизлияния на коже, слизистых оболочках и глазном дне, носовые, десневые, маточные, кишечные, почечные и другие кровотечения. При прогрессировании процесса может иметь место неврологическая симптоматика, обусловленная геморрагиями в головной мозг. При парциальной Г. а. кровоточивость отсутствует. Размеры лимфатических узлов, селезенки и печени не изменяются.
Картина крови. Анемия носит нормохромный, нормоцитарный, реже макроцитарный характер. Полихроматофилия отсутствует, число ретикулоцитов нормально или снижено. Лейкопения может достигать 1000 клеток в 1 мкл и менее; она обусловлена в основном гранулоцитопенией и сопровождается относительным лимфоцитозом. Абсолютное число лимфоцитов при резкой лейкопении также снижено. Отмечается тромбоцитопения с удлинением времени кровотечения (см.) и снижением ретракции кровяного сгустка (см. Ретракция). Плазменные факторы свертывания крови (см. Свертывающая система крови) не изменяются. Содержание сывороточного железа повышено, общая железосвязывающая способность сыворотки чаще повышена.
Парциальная Г. а. характеризуется хрон, нормоцитарной анемией, часто без лейко- и тромбоцитопении, с глубокой ретикулоцитопенией.
Пунктат костного мозга, как правило, скудный, ядерные элементы представлены в основном лимфоцитами, немногочисленными гранулоцитами и нормобластами. Мегакариоциты чаще отсутствуют. Иногда, несмотря на явную панцитопению, пунктат оказывается довольно богатым; это связано с попаданием иглы в очаг сохранившегося кроветворения. Помимо чисто количественного дефицита эритробластических элементов, при Г. а. отмечают признаки качественной их патологии (дизэритропоэз), мегалобластоидность, атипичные митозы, многоядерность (см. Дизэритропоэтическая анемия). При парциальной Г. а. пунктат костного мозга богат ядерными элементами, лейко-тромбоцитопоэз не нарушен, но число клеток красного ряда нередко резко уменьшено или они полностью отсутствуют.
Рис. 3. Микропрепарат костного мозга подвздошной кости (гипопластическая анемия): резкое преобладание жирового костного мозга над кроветворным. Костномозговые полости заполнены преимущественно жировой тканью, миелоидная ткань представлена маленькими островками черного цвета; х 280.
Трепанобиопсия подвздошной кости выявляет резкое преобладание жирового костного мозга над кроветворным (рис. 3), иногда отсутствие последнего.
Исследование с радиоактивным железом 59Fe дает наиболее точную суммарную оценку эритропоэза: клиренс изотопа из плазмы замедлен, он накапливается в основном в печени, включение метки в эритроциты резко замедлено.
Приобретенная АА
Приобретенная апластическая анемия – такое состояние кроветворного органа, которое взялось как бы ниоткуда: семейный анамнез ничего плохого не предполагал, среди близких (да и дальних тоже) родственников больных нет, каких-то врожденных дефектов и аномалий у пациента не отмечается. Но в главном органе кроветворной системы производство клеток всех линий, циркулирующих в кровеносном русле и обеспечивающих нормальную жизнедеятельность организма, почему-то приостановилось. Возникшая в процессе жизни апластическая анемия, может быть представлена 4 видами:
- Идиопатическая апластическая анемия (причинные факторы, пусть при самом детальном обследовании, обозначить не представляется возможным) – составляет более 50% всех АА (по данным разных источников – от 50 до 80%);
-
Вирусная АА (парвовирус В19, вирус Эпштейн-Барра, гепатитов);
- Аутоиммунная АА – болезнь обусловлена влиянием на кроветворные клетки аутоагрессивных (аутологичных) антител (аутоантитела – АТ, способные реагировать на собственные антигены);
- Транзиторная (временная) гипопластическая анемия – чаще всего отмечается у детей, дифференцируется с врожденной ГА и среди других костномозговых аплазий (у детей) занимает лидирующее положение, причина – временное (транзиторное) угнетение кроветворения в костном мозге, но на выздоровление при адекватном лечении можно рассчитывать через 1-2 месяца.
Для приобретенных АА также обозначены три формы течения с характерными для каждой из них четкими клинико-гематологическими особенностями:
- Сверхтяжелая форма (как правило, это острая апластическая анемия, которая развивается стремительно и дает практически 100% летальность);
- Тяжелая;
- Легкая форма, если можно так назвать, скорее, нетяжелая, что несколько меняет смысл, подразумевая удовлетворительное состояние кроветворения и самочувствие пациента.
Приобретенные аномалии стволовых клеток, дающих жизнь всему сообществу форменных элементов, могут возникать по разным причинам, основные из которых будет нелишним рассмотреть.
Методы лечения
Лечение апластической анемии — сложный и комплексный процесс, требующий активного участия врача и пациента. Для медикаментозной терапии могут применяться следующие группы лекарств:
- Антибиотики (Амикацин, Цефтриаксон, Тобрамицин). Назначаются при присоединении бактериальной инфекции.
- Цитостатики (Имуран, Метотрексат, Циклофосфан). Назначают для лечения приобретённых форм апластической анемии.
- Иммунодепрессанты (Метилпреднизолон, Дексаметазон). Уменьшают реакцию иммунитета, позволяя костному мозгу вырабатывать кровяные клетки.
- Стимуляторы кроветворения (Нейпоген, Лейкин). Усиливают выработку кровяных клеток костным мозгом.
Единственным радикальным способом, позволяющим взять под контроль апластическую анемию и получить положительный результат, является трансплантация костного мозга. Такая методика наиболее эффективная в молодом возрасте, но есть одна сложность — материал для пересадки должен быть совместим или частично совместим с антигенным составом костного мозга больного. В этом случае лучше всего подходит ближайший родственник пациента.
Для лечения патологии, сопровождающейся низким значением эритроцитов или тромбоцитов, можно применять переливание крови. Методика не позволяет избавить от апластической анемии, но заболевание будет взято под контроль специалистов, что положительно скажется на самочувствии больного.
Лечение апластической анемии
Лечение идиопатической и других видов апластической анемии – очень сложная задача, требующая комплексного индивидуального подхода. При разработке тактики специалисты ЦЭЛТ учитывают результаты диагностики и показания пациента. Больного помещают в изолятор с асептическими условиями, что позволяет исключить риск развития инфекций и их осложнений. Медикаментозная терапия заключается в приёме:
- Глюкокортикоидов – при выявлении аутоиммунных механизмов и формировании антител против собственных кровяных клеток;
- Цитостатиков – при отсутствии эффекта от лечения глюкокортикоидами при аутоиммунной анемиии;
- Циклоспорина «А» – для подавления производства ФНО и интерферона “y”;
- Анаболиков – для стимулирования функции кроветворения;
- Андрогенов – для стимулирования образования красных кровяных клеток.
Всем больным апластической анемией проводят переливание эритроцитарной и/или тромбоцитарной массы, в объёмах, определяемых исходя из клинической картины и показателей периферической крови. Кроме того, пациенту могут назначить спленэктомию – хирургическое вмешательство, направленное на удаление селезёнки. Самые благоприятные прогнозы может обеспечить трансплантация костного мозга. Она заключается в пересадке донорских или собственных стволовых кроветворных клеток, предварительно изъятых из подвздошных костей путём пункции. К сожалению, процедура недоступна для широкого применения из-за сложности подбора совместимого донора. В том случае, если это невозможно, пациенту назначают паллиативную терапию с применение циклоспорина А.
В отделении гематологии нашей клиники ведут приём кандидаты, доктора и профессоры медицинских наук с опытом практической и научной работы от двадцати пяти лет. Вы можете записаться к ним на приём онлайн или обратившись к нашим операторам. Специалисты высокой квалификации работают и в отделении . К ним можно записаться на
В ЦЭЛТ вы можете получить консультацию гематолога.
- Первичная консультация — 3 200
- Повторная консультация — 2 000
Записаться на прием
Записавшись на прием гематолога, вы сможете получить всестороннюю консультацию. В компетенции врача находится лечение различных заболеваний крови, большинство из которых можно выявить на ранних стадиях и назначить своевременное лечение, позволяющее справиться с болезнью быстро и легко.
Наши врачи
Тюкалова Наталья Рудольфовна
Врач-гематолог, педиатр, кандидат медицинских наук
Стаж 28 лет
Записаться на прием
Дворецкий Леонид Иванович
Врач-терапевт, гематолог, доктор медицинских наук, профессор
Записаться на прием
Лабораторные исследования
- Клинический анализ крови — 950
руб. - Коагулограмма развернутая — 2 000
руб. - Обмен железа (железо несвязанное, трансферин) — 700
руб. - Витамин В 12 — 650
руб. - Фолиевая кислота — 650
руб. - Цитологическое исследование пунктатов (1 локализация) — 1 900
руб. - Цитологическое исследование пунктатов щитовидной железы и других органов и тканей (1 локализация) — 1 900
руб. - Гистологическое исследование биопсийного материала лимфоузлов — 3 500
руб. - Гистологическое исследование биопсийного материала ткани костного мозга — 4 500
руб.
- (печень, желчный пузырь, поджелудочная железа, селезенка) — 3 800 руб.
- УЗИ лимфатических узлов, комплексное (несколько регионов) — 3 000 руб.
- Ультразвуковое исследование и компрессионная поверхностных лимфатических узлов — 4 000 руб.
Рентгенологические исследования
Рентгенография органов грудной клетки (обзорная) — 2 500 руб.
Компьютерная и
- гепато-панкреато-дуоденальной области и селезенки — 11 000 руб.
- МР томография органов брюшной полости (печень, желчный пузырь, поджелудочная железа, селезенка) с внутривенным введением контрастного вещества — 14 000 руб.