Синдром рея
Содержание:
Причины (этиология)
Синдром Драве связан с мутацией в гене SCN1A в 80-90% случаев. Усовершенствованное генетическое тестирование, включая дублирование, удаление и идентификацию мозаицизма, продолжает увеличивать этот процент. Миссенс (40%), нонсенс (20%), сдвиг кадров (20%), дупликации/делеции (7%) и мутации места сплайсинга (10%) были связаны с синдромом Драве.
Более легкие проявления (фенотипы) состояний, связанных с SCN1A, чаще связаны с ошибочными мутациями, но ни тип мутации, ни местоположение на гене не соответствуют клинической тяжести СД.
90% мутаций, по-видимому, являются новыми для ребенка и не унаследованы от родителя. В документированных случаях унаследованных мутаций SCN1A родитель имеет более легкую форму эпилепсии или неврологические симптомы отсутствуют, тогда как у ребенка проявляется СД. Усовершенствованное тестирование обнаружило мозаичные мутации у родителей, которые ранее дали отрицательный результат на SCN1A мутации. Мозаизм — это состояние, при котором некоторые клетки человека генетически отличаются от других клеток этого человека. Это может произойти вскоре после оплодотворения, когда отдельная клетка в скоплении клеток подвергается спонтанной мутации. Только клетки, происходящие из этой мутированной клетки, будут нести мутацию: немутантные клетки будут давать здоровые клетки, и, таким образом, развитый индивидуум может иметь слегка различную структуру своих клеток.
Риск рецидива составляет 50% в семьях с наследственными мутациями SCN1A. Из-за выявления мозаицизма и возможности мутаций в яйцеклетках или сперматозоидах (мутации зародышевой линии) риск рецидива даже для явно новых мутаций повышен по сравнению с обычным населением, и поэтому рекомендуется генетическое консультирование.
Другие гены связанные с СД, включая SCN2A, SCN8A, GABRA1, GABARG2, PCDH19, STXBP1 и SCN1B, но клиническая картина в этих случаях часто несколько нетипична для синдрома.
Диагностика
Поскольку синдром Рея не имеет патогномоничных симптомом, диагностика его сложна. Заподозрить патологию педиатру позволяют данные анамнеза: связь с вирусной инфекцией и приемом «Аспирина». Для подтверждения или опровержения диагноза проводят ряд лабораторных и инструментальных методов исследования.
- Общий анализ крови — гипогликемия, незначительный лейкоцитоз.
- Биохимия – повышение в крови маркеров печеночной патологии — АЛТ и АСТ, гипераммониемия, гипоальбуминемия.
- Коагулограмма — гипопротробинемия.
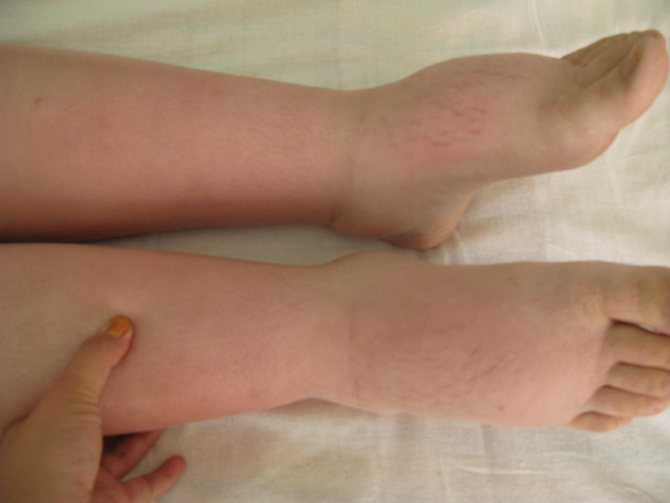
- Ультразвуковое исследование внутренних органов — гепатомегалия, снижение эхогенности и нечеткость контуров поджелудочной железы.
- Биопсия печени – диффузная жировая дистрофия гепатоцитов, отсутствие воспалительных инфильтратов.
- Исследование ликвора определяет его стерильность, что позволяет исключить инфекционный характер энцефалопатии.
- Электроэнецефалография.
- Томографическое исследование.
Причины и патогенез
Причины формирования болезни не изучены до конца. Однако, ученые считают, что в основе патогенеза лежат два процесса. Это усиление синтеза фактора некроза опухолей под действием вируса и препарата АСК. И нарушение процессов бета-окисления с накоплением внутри клетки жирных кислот. А также прекращение окислительного фосфорилирования из-за патологического влияния метаболитов ацетилсалициловой кислоты на каналы в митохондриях.
Аспирин (ацетилсалициловая кислота, АСК)
Этот препарат является одним из самых «старых» нестероидных противовоспалительных средств. Используется он для подавления воспаления в организме: боли, жара, отека, нарушения функции органа.
Действует аспирин, подавляя синтез простагландинов (активаторов
воспаления) из арахидоновой кислоты. Ферментирует (активизирует) этот процесс
циклооксигеназа. Именно его и блокируют все НПВС.
А также доказано, что циклооксигеназа представлена в двух формах. Это ЦОГ-1, которая подавляет синтез простогландинов, регулирует целостность слизистой ЖКТ, управляет активностью тромбоцитов и почечным кровотоком. И ЦОГ-2, которая только подавляет синтез простогландинов.
АСК тропна только к первому изоферменту, поэтому у
лекарства большое количество побочных эффектов. Кроме того, у аспирина
выраженное дозозависимое действие.
- Доза 325 мг используются для дезагрегантной терапии;
- Доза 1,5-2 грамма используется для снятия жара и воспаления;
- Доза больше 4 грамм оказывает выраженное противовоспалительное действие.
Ветрянка
Это вирусное заболевание, которое отличается высокой заразностью. Передается болезнь воздушно-капельным или контактным путем. В острой фазе появляется лихорадка и папуловезикулярная сыпь.
Возбудителем ветрянки является герпес-вирус третьего типа. Это еще называют Varicella zoster. Вирус поселяется в ганглиях нервной системы человека и до конца жизни остается с ним. В пожилом возрасте он может провоцировать острое состояние, называемое «опоясывающий лишай».
У детей герпетические болезни (ветрянка) протекают доброкачественно. Для снятия жара можно использовать свечи с парацетамолом или сиропы Ибупрофен. Категорически запрещено принимать аспирин. Везикулы следует обрабатывать любой дезинфицирующей жидкостью или мазью (Каламин).
Грипп
Грипп вызывают несколько разновидностей вирусов. Выделяют
грипп А, В и С. Синдром Рея, как правило, появляется при назначении салицилатов
детям до 12 лет с инфекцией типа А и В.
Чаще всего синдром Рея при гриппе фиксируют в возрастной группе от 4 до 14 лет. Первые признаки болезни появляются на 3-и сутки после приема салицилатов в терапевтических дозах.
Клиническая картина характеризуется рвотой, тошнотой. Она повторяется несколько раз. После нее в течение суток нарастают неврологические симптомы. Они варьируют от легких расстройств моторики и психики до комы.
Стадии
Нулевая стадия протекает незаметно. Ее можно определить только на основании лабораторных изменений. Клинических симптомов не наблюдается. В крови повышены АЛТ, АСТ, уровень аммиака.
На первой стадии клиника характеризуется вялостью и сонливостью у ребенка. Появляются рвота и тошнота. Изменяется скорость волн на ЭЭГ. Уровень аммиака в крови нормализуется.
На второй стадии ребенок проявляет агрессивность, возбуждение, тревожность. При осмотре отмечается гиперрефлексия, замедленная реакция зрачков на свет, ответ на стимуляцию отсутствует. Еще больше замедляются волны на ЭЭГ.
Третья стадия – это наступление коматозного состояния. Характеризуется неадекватной реакцией на раздражители. Чувствительность снижена, зрачки реагируют на свет. Наступает дисфункция печени. ЭЭГ регистрирует медленные дельта волны с высоким вольтажом.
На четвертой стадии наступает глубокая кома. Зрачки не реагируют на свет, пропадают окуловестибулярные рефлексы. На ЭЭГ понижается вольтаж дельта волн. Печеночная недостаточность не прогрессирует.
Пятая стадия характеризуется появлением изолинии на ЭЭГ. У пациента возникают судороги, потеря тонуса и рефлексов. Нет дыхания и реакции на свет.
Лечение синдрома Рея
Согласно сообщениям в медицинской литературе, основы лечения включают:
- раннюю диагностику;
- быстрое введение интенсивной терапии по мере необходимости;
- меры по исправлению метаболических нарушений;
- меры по предотвращению или контролю повышенного давления между черепом и мозгом (внутричерепного давления), вторичного к отеку головного мозга.
Конкретные методы лечения могут варьироваться от человека к человеку, в зависимости от тяжести заболевания и прогрессирования. Например, у детей с легкими заболеванием (например, I стадии) лечение может в основном состоять из тщательного наблюдения. Однако, в случаях с более тяжелым заболеванием может потребоваться интенсивное неотложное лечение. Такие меры могут включать:
- постоянный мониторинг жизненно важных функций (например, кровообращения, баланса жидкости/электролита, дыхания);
- доставка жидкостей, электролитов и глюкозы через вену (внутривенно);
- использование респиратора для облегчения дыхания.
Уровни внутричерепного давления также должны тщательно контролироваться, и некоторые лекарства (например, маннит, дексаметазон) могут вводиться, чтобы помочь контролировать отек мозга и уменьшить внутричерепное давление.
Дополнительные меры могут включать:
- введение клизмы с антибиотиком (неомицин) и агента, способствующего удалению аммиака из крови (например, лактулозы);
- лечение витамином К или переливание крови (например, тромбоцитами или свежезамороженной плазмой) при нарушениях свертываемости крови;
- использование охлаждающего одеяла или других методов для стабилизации или предотвращения ненормально повышенной температуры тела (гипертермии);
- и/или другие меры.
Для некоторых больных с расстройством могут быть рекомендованы дополнительные симптоматические и поддерживающие меры.
Ученные указывают, что, по-видимому, существует корреляция между остаточными когнитивными эффектами и тяжестью неврологического ухудшения после начала терапии.
Люди с легким заболеваниями (например, I стадией) обычно полностью выздоравливают. Тем не менее, люди с более тяжелым заболеванием могут иметь остаточные неврологические симптомы, такие как умственная отсталость, трудности с формированием мыслей и визуальных и двигательных функций, или другие связанные с этим аномалии.
Необходимо соблюдать большую осторожность при назначении обезболивающих препаратов пациентам с подозрением на эпизод синдрома Рея. Пациенты и их семьи должны обсудить со своими врачами причины выбора определенных обезболивающих препаратов
Лечение
Основными целями терапевтических мероприятий являются:
- Борьба с отеком мозга и энцефалопатией,
- Коррекция метаболизма,
- Восстановление нарушенных показателей свертываемости крови.

Всем больным проводят симптоматическое лечение, направленное на устранение неприятных проявлений болезни, доставляющих больному ощутимый дискомфорт и существенно нарушающих качество жизни.
Пациентам назначают:
- Кортикостероидные средства – «Преднизолон», «Бетаметазон», «Дексаметазон» и их производные.
- Внутривенное введение коллоидных и кристаллоидных растворов для уменьшения интоксикации и выведения продуктов метаболизма из организма.
- Диуретики для снятия отека мозга – «Маннитол», «Фуросемид», «Лазикс».
- Противосудорожные лекарства для предупреждения судорог – «Фенитоин».
- Ограничение рвоты при помощи «Метоклопрамида» и «Церукала».
- Интубация трахеи и искусственная вентиляция легких при дыхательных нарушениях.
- Лечение кровотечений – переливание тромбоцитарной массы и плазмы.
- Гемодиализ — для коррекции ацидоза и гипераммониемии.
- В тяжелых случаях выполняется трансплантация печени.
При выявлении первых признаков патологии не рекомендуют заставлять ребенка принимать пищу. Необходимо настаивать на употреблении воды, травяного чая, морса или любой другой жидкости, поскольку рвота с поносом могут быстро привести к обезвоживанию детского организма.
 Единственным профилактическим средством при синдроме Рея является полный отказ от приема «Аспирина» и препаратов, в состав которых он входит. Детям до 12 лет для лечения лихорадки рекомендуют принимать средства на основе парацетамола или ибупрофена.
Единственным профилактическим средством при синдроме Рея является полный отказ от приема «Аспирина» и препаратов, в состав которых он входит. Детям до 12 лет для лечения лихорадки рекомендуют принимать средства на основе парацетамола или ибупрофена.
Прогноз патологии определяется степенью повреждения мозговой и печеночной ткани. Легкая форма синдрома Рея в 100% случаев заканчивается полным выздоровлением и восстановлением психоневрологического состояния больных детей. Быстро прогрессирующие гепатологические и метаболические расстройства увеличивают риск впадения пациента в кому.
Воспаление и отек головного мозга, быстрое поражение печеночной ткани и скопление в ней жира — основные патологические процессы, протекающие при синдроме Рея. При выявлении клинических признаков на ранней стадии болезни прогноз всегда благоприятный. Именно поэтому важным является своевременное обращение к специалистам. Только быстрая диагностика и адекватная терапия являются основой успешного исхода болезни.
Прогнозы по синдрому Рейе
Только быстрая диагностика и своевременно проводимая терапия являются основой успешного исхода болезни. В последнее время уровень смертности больных с диагнозом синдром Рейе заметно снизилась, но дети грудного возраста и пациенты в 4 стадии течения рассматриваемой патологии являются исключением.
Если говорить о прогнозе заболевания, то он зависит только от степени изменений функций центральной нервной системы и скорости прогрессировании нарушений. Если пациент преодолел острую фазу патологии, то в большинстве случаев наступает его полное выздоровление. В некоторых случаях могут проявляться признаки повреждения клеток головного мозга – например, у ребенка начинается задержка умственного развития, периодически возникающие судороги, патологии периферических нервов.
Неблагоприятный прогноз по синдрому Рейе имеет свои отличительные признаки – у больного происходит стремительная смена первых трех стадий, судороги появляются на ранней стадии, внутричерепное давление резко повышается.
Обратите внимание: синдром Рейе практически никогда не развивается у одного человека дважды. Этот факт врачи тоже пока не могут объяснить
Конечно же, стоит знать и правила профилактики синдрома Рейе – такое заболевание точно легче предупредить, чем потом лечить. Во-первых, нужно внимательно следить за состоянием здоровья ребенка или взрослого, которые находятся на этапе развития вирусной инфекции. При первых же проявлениях проблем в работе органов желудочно-кишечного тракта нужно немедленно обращаться за квалифицированной медицинской помощью, а не заниматься самолечением. Во-вторых, нужно исключить из терапии вирусных инфекций препараты ацетилсалициловой кислоты (Аспирин, в частности).
Синдром Рейе – опасное и «коварное» заболевание. Да, встречается оно редко, но может развиться у каждого ребенка и взрослого на фоне протекающих вирусных инфекций. Современная медицина в состоянии помочь больным с рассматриваемой патологией, но для этого нужно провести своевременную диагностику. А учитывая вероятность развития осложнений на фоне поражений головного мозга, гораздо проще будет предпринять необходимые профилактические меры и избежать развития синдрома Рейе.
Цыганкова Яна Александровна, медицинский обозреватель, терапевт высшей квалификационной категории
9, всего, сегодня
(50 голос., средний: 4,44 из 5)
презентация
- Этот синдром обычно возникает у ребенка с непримечательной историей болезни, через 3-5 дней после фазы выздоровления от неисключительной вирусной болезни.1Чаще всего это инфекция верхних дыхательных путей, грипп, ветряная оспа или гастроэнтерит. Другие вирусные заболевания могут быть связаны.
- Типичный пациент резко ухудшается, обычно через три дня после явного улучшения. Первоначально наблюдается длительная рвота (редко это может отсутствовать), сопровождаемая вялостью, вялостью и сонливостью через 24–48 часов. Это связано с тахипноэ. Использование противорвотных средств связано с этиологией и может осложнить презентацию, маскируя рвотный аспект презентации.
- Первым признаком у более молодых пациентов (в возрасте до 2 лет) могут быть просто диарея и тахипноэ.
- Пациент может продолжать ухудшаться с более выраженными неврологическими симптомами. Изначально это может быть изъятое государство. За ним следуют бред и растерянность, боевое поведение и ступор. Могут быть визуальные галлюцинации.
- Могут быть вялые зрачковые реакции, но офтальмологические особенности повышенного ICP не всегда присутствуют.
- Клиническое ухудшение может продолжаться, иногда прогрессируя до судорог и комы. Умеренная поза, опистотонус, расширенные / неравные зрачки, учащенное дыхание, изменения пульса и, наконец, вялое апноэ, предшествующее смерти.
Функция печени нарушается, иногда с легкой гепатомегалией, но без желтухи. Течение болезни может варьироваться (4-60 часов), а неврологический статус может стабилизироваться или улучшаться (самопроизвольно или с помощью терапии) на любой стадии, за исключением смерти мозга.
У детей с преобладающими респираторными симптомами и признаками (тахипноэ, респираторный дистресс, гиперинфляция и апноэ) ± температурной нестабильностью. Гипогликемия и гепатомегалия встречаются чаще, рвота обычно отсутствует. История предшествующей вирусной инфекции встречается реже.
Лабораторные данные
Выявление патологических отклонений при лабораторных исследованиях подтверждает наличие СР. Предлагаются нижеследующие лабораторные исследования.
1. Печеночные функциональные тесты. Комплекс печеночных тестов включает определение протромбинового времени, частичного тромбопластинового времени (пролонгированного), сывороточной активности ГОТ и ГПТ (в 2—20 раз выше нормы), сывороточного аммиака (превышение нормы в 2—20 раз) и билирубина (обычно в пределах нормы). В отсутствие аномальных показателей печеночных функциональных тестов или при определении повышенного уровня билирубина (общий билирубин более 5 мг/дл) подтверждение диагноза СР представляется достаточно трудным.
Бесспорным признаком синдрома Рейе является повышение уровня аммония в крови. Хотя четкой корреляции между этим показателем и исходом синдрома не отмечается, уровень аммиака выше 350 мг/дл (в венозной крови) ассоциируется с плохим прогнозом.
Повышенное содержание аммиака в крови отражает нарушения в цикле мочевины. Именно в митохондриальном матриксе локализуются два фермента, участвующие в метаболизме мочевины: карбамилфосфатсинтетаза и орнитин-карбамилтрансфераза.
Преходящее повышение показателей печеночных функциональных тестов может наблюдаться при связанном с ветрянкой гепатите даже в отсутствие СР.
При СР показатели печеночных тестов нормализуются в течение 3—5 дней. Эта быстрая нормализация помогает в дифференциации синдрома Рейе и острой желтой атрофии вследствие гепатита или отравления.
2. Креатинфосфокиназа. Уровень креатинфосфокиназы (КФК) при СР также повышен. Причем это относится к ее ММ-фракции (скелетная мускулатура), МВ-фракции (сердце), но не к ВВ-фракции (мозг). Степень повышения активности КФК коррелирует с тяжестью и исходом заболевания: у больных с наибольшей активностью КФК отмечается наиболее высокая смертность.
3. Уровень глюкозы в крови. Гипогликемию поначалу считали важнейшим симптомом СР. В настоящее время установлено, что она имеет место у 40 % заболевших детей, обычно до 5-летнего возраста и особенно у младенцев до 1 года. Низкий уровень сахара в крови коррелируют с плохим исходом заболевания; он обусловлен уменьшением запасов гликогена и увеличением утилизации сахара, что часто наблюдается при повышенном содержании аммиака в крови.
4. Электролиты сыворотки и азот мочевины крови. Их содержание либо остается нормальным, либо изменяется, отражая степень дегидратации, обусловленной анорексией и рвотой. Исходные показатели этих параметров должны быть получены до начала лечения с ограничением приема жидкости и применением диуретиков.
5. Полный клинический анализ крови с определением числа лейкоцитов и тромбоцитов. Эти параметры обычно остаются в пределах нормы. Число лейкоцитов может быть повышенным вследствие стресса или метаболического ацидоза. Количество тромбоцитов изредка бывает пониженным.
6. Активность амилазы. Уровень амилазы повышается примерно у 4 % детей с синдромом Рейе, что связано с вовлечением в патологический процесс поджелудочной железы.
7. Анализ мочи. Он проводится с целью оценки исходного состояния мочи до лечения с ограничением жидкости и применением диуретиков.
8. Люмбальная пункция. Люмбальная пункция рекомендуется для исключения инфекционного поражения ЦНС. Правда, существуют некоторые противоречия в отношении показаний к ее проведению у детей с предполагаемым повышением внутричерепного давления. Результаты исследования спинномозговой жидкости (СМЖ) обычно бывают нормальными; иногда определяется несколько пониженный уровень глюкозы или слабо выраженный моноцитоз.
9. КТ-сканирование. КТ-сканирование выявляет диффузный отек мозга при уплощенной форме желудочков.
10. ЭКГ. ЭКГ может обнаружить аритмию или признаки миокардита, хотя они обычно бывают слабо выраженными и не требуют лечебных мероприятий.
11. Другие лабораторные исследования. Они включают определение аномального соотношения аминокислот в крови, повышенного уровня свободных жирных кислот (сывороточные дикарбоксиловые кислоты) при сниженном содержании липидов, а также выявление респираторного алкалоза, метаболического ацидоза и кетонурии.
Описание1
Это редкий синдром, характеризующийся острой, опасной для жизни, невоспалительной энцефалопатией и жировой дегенерацией печени с минимальными или отсутствующими клиническими признаками поражения печени. При классическом синдроме Рейе наблюдается серьезное, но самоограничивающееся нарушение структуры митохондрий и связанные с ним ферментативные нарушения, обычно продолжающиеся около шести дней. Это сопровождается интенсивным, острым катаболическим состоянием, связанным с отеком мозга при отсутствии энцефалита или менингита.
Патогенез синдрома Рейе неясен, но, по-видимому, он включает митохондриальную дисфункцию, которая ингибирует окислительное фосфорилирование и бета-окисление жирных кислот у зараженного вирусом сенсибилизированного хозяина. Хозяин обычно подвергался воздействию митохондриальных токсинов, чаще всего салицилатов (> 80% случаев). Гистологически митохондрии становятся опухшими и уменьшенными в количестве. Печень и почка поражены. Изменения в мозге приводят к отеку головного мозга и повышению внутричерепного давления (ICP).
Это состояние является очень редким осложнением распространенных вирусных инфекций. Это часто происходит после ничем не примечательной вирусной инфекции, особенно после гриппа B, гриппа A, ветряной оспы или парвовирусных инфекций.2 Также сообщалось после гастроэнтерита и даже вакцин против живых вирусов. Корь не замешана. Считается, что он возникает в результате взаимодействия между вирусными и токсическими факторами окружающей среды, причем наиболее вероятным механизмом является взаимодействие токсических веществ в митохондриях, сенсибилизированных вирусной инфекцией.
Наиболее интенсивно исследованным токсическим фактором был салицилат (обычно в форме аспирина).3Это произошло из-за эпидемиологических ассоциаций (аспирин встречается в> 80% случаев, хотя это не было географически универсальным) и из-за гистопатологического сходства между изменениями печени при синдроме Рейе и при остром отравлении салицилатом.
Другие препараты, которые использовались у пациентов с синдромом Рейе, включали устаревшие тетрациклин, вальпроевую кислоту, зидовудин, диданозин и противорвотные средства. Синдром Рейе или синдром Рейе-подобного также связан с инсектицидами, гербицидами, афлатоксинами, краской, разбавителем краски, маслом маргозы, гепатотоксическими грибами, гипоглицином у плодов аки (ямайская рвота) и травяными препаратами с атрактилозидом (дитерпеноидным гликозидом, обнаруженным в экстракты клубня Callilepis Laureola — отравление импилой).
Рей-подобные заболевания также были описаны, в результате чего наблюдается сходная патологическая картина, но связанная с наследственными нарушениями обмена веществ, такими как дефекты цикла мочевины, дефицит альфа-1-антитрипсина, фруктоземия и т. Д.4 Нарушения метаболизма жирных кислот, по-видимому, более выражены. Число этих расстройств, о которых сообщалось, что они имеют синдром Рейе, увеличивается. Муковисцидоз является одним из таких состояний. В настоящее время считается, что синдром Рейе встречается очень редко, и любой ребенок с таким заболеванием должен проходить тестирование на наличие врожденных нарушений обмена веществ.5 Это, безусловно, правда, что, поскольку запрет на использование аспирина в возрасте до 12 лет в 1986 году, он снизился, и утверждается, что лучшая диагностика метаболических нарушений не будет объяснять все это. Возможно, что вовлечены другие факторы, пока неизвестные — изменение генетического кода вируса обсуждалось.1 В 2002 году запрет на аспирин был повышен до 16 лет.6
В 2008 году в Британском медицинском журнале был опубликован отчет о применении салицилатсодержащего орального геля у пациента с подозрением на синдром Рейе. Хотя в конечном итоге этот случай был диагностирован как салицилатная токсичность, тот факт, что в крови пациента был обнаружен значительный уровень препарата, привел к тому, что Агентство по охране здоровья выпустило предупреждение об использовании салицилатных оральных гелей у детей до 16 лет. Были затронуты следующие продукты: Bonjela и Bonjela Cool Mint. Также было выпущено предупреждение о Pyralvex, краске, используемой для зубной боли / язвы в полости рта.7
управление
Успешное лечение заболевания зависит от ранней диагностики. Он направлен на предотвращение, коррекцию и минимизацию метаболических нарушений и контроль над повышенным ВЧД. Раннее распознавание и лечение необходимы для предотвращения смерти и неврологических нарушений на протяжении всей жизни.
Здесь описаны важные аспекты управления, но они не подходят (или не возможны) в первичной помощи. Задача врача общей практики состоит в том, чтобы распознать состояние на ранней стадии и срочно обратиться к нему.
- Стоит отметить, что пациент должен быть как можно тише; ненужное обращение или стимуляция повышает ICP.
- Установите и поддерживайте дыхательные пути пациента, дыхание и кровообращение по мере необходимости.
- Проверьте уровень глюкозы, особенно если пациент моложе 1 года, имеет измененный психический статус или оба. Администрирование декстроза для управления гипогликемией.
Не существует специального лечения синдрома Рейе. Лечение поддерживающее. При поступлении некоторые из шагов, предпринятых в начальном управлении, будут включать:
Поддержание дыхательных путей и оксигенации мозга.
Немедленная коррекция любой гипогликемии с помощью внутривенного введения глюкозы и настройка 10% инфузии глюкозы. Уровень сахара в крови должен быть между 11 ммоль / л и 22 ммоль / л (т.е
выше, чем обычно).
Если артериальное давление в норме, голову и верхнюю часть туловища следует поднять под углом 40 ° и избегать чрезмерного увлажнения.
Мониторинг и контроль химического состава крови и предотвращение обезвоживания.
Ондансетрон может быть осторожно использован для контроля рвоты. Антациды также могут быть предписаны.
Гипераммонемию можно лечить фенилацетатом натрия / бензоатом натрия или гемодиализом.
Контроль лихорадки.
Противосудорожные препараты (например, фенитоин) могут потребоваться для лечения судорог (если они используются в острой фазе, они, вероятно, потребуются в течение нескольких месяцев после выздоровления).
Исправление дефектов коагуляции, если PTT превышает 16 секунд; витамин К может понадобиться для исправления кровотечения.
С коллегами-экспертами следует проконсультироваться заблаговременно и получить разрешение на прием в МСЭ.
Стадия 2 или хуже требует направления в третичный центр, где можно контролировать и снижать ICP с помощью соответствующей терапии. Другие параметры (центральное венозное давление, нарушения биохимии крови, коагулопатии, судороги и т. Д.) Также необходимо тщательно контролировать.
Сообщалось о случае молниеносного гепатита, успешно вылеченного с помощью трансплантации печени.9
Признаки и симптомы

Симптомы синдрома Рея обычно начинаются после вирусного заболевания, особенно инфекции верхних дыхательных путей (например, вирусом гриппа B) или, в некоторых случаях, ветряной оспы. Реже синдром Рейе может развиться после заражения другими вирусными агентами, такими как грипп A или краснуха.
Приблизительно через 3-5 дней после появления вирусной инфекции у больных детей возникает внезапная, постоянная неконтролируемая рвота. Далее возникают нарушения сознания, они могут начаться одновременно или развиваться в течение нескольких часов. Такие расстройства сознания часто включают:
- раздражительность;
- беспокойство;
- дезориентацию;
- вялость и ухудшение памяти.
Некоторые дети могут оставаться вялыми без прогрессирования до потери сознания. В других случаях неврологическое ухудшение может быть быстро прогрессирующим, приводя к:
- очевидному отсутствию осведомленности об окружающей среде (ступор);
- состоянию бессознательного состояния и безразличия (кома);
- расширению зрачков (мидриаз);
- учащенному, неглубокому дыханию (тахипноэ);
- учащенному сердцебиению (тахикардия);
- потере определенных рефлексов (например, глубоких сухожилий, зрачков, окулоцефальных (феномен головы и глаз куклы)).
Тяжелая неврологическая дисфункция может также привести к:
- эпизодам неконтролируемых электрических нарушений в мозге (эпилепсия);
- ненормальной осанке (децеребрационная и декортикационная ригидность), указывающая на повреждение определенных участков мозга;
- потенциально опасным для жизни осложнениям.
Признаки, связанные с жировой дегенерацией печени, могут включать увеличение печени (гепатомегалия) и ненормально повышенные уровни некоторых ферментов печени (печеночных трансаминаз), что указывает на нарушение функции печени. Тем не менее, желтуха, часто ассоциирующееся с дисфункцией печени, обычно не проявляется или является минимальной у лиц с расстройством.
У людей с синдромом Рейе тяжесть заболевания может быть крайне вариабельной. Согласно сообщениям в медицинской литературе, некоторые больные могут иметь легкие симптомы без прогрессирования заболевания. Однако, как обсуждалось выше, у других людей с расстройством может развиться быстрое неврологическое ухудшение, приводящее к потенциально опасным для жизни последствиям.
Ученные предложили клиническую систему стадирования, основанную на различных уровнях тяжести болезни, причем I, II и III стадия указывают на относительно легкую или умеренную болезнь, а IV и V стадии указывают на более тяжелую болезнь.
Острая печеночная энцефалопатия
Печеночная энцефалопатия развивается при остром или хроническом заболевании печени. В результате болезни формируется комплекс синдромов, поражающих головной мозг. Это и отек мозга, и необратимые изменения в коре. Заболевание может протекать в легкой форме, а может заканчиваться тяжелой инвалидностью и смертью.
МКБ-10
В международной классификации болезней 10-го пересмотра синдром Рея относится к заболеваниям нервной системы.
| Шифр | Наименование болезни |
| G00-G99 | Болезни нервной системы |
| G90-99 | Другие нарушения нервной системы |
| G93 | Другие поражения головного мозга |
| G93.7 | Синдром Рейе или Рея |
Прогноз
Синдром Рея характеризуется острым течением. Детская летальность составляет при нем около 20%. Если болезнь протекает в легкой форме, то у 80% детей полностью восстанавливаются мозговые функции. Но если нарушения печени тяжелые, а пациент впадает в кому, то вероятность плохого прогноза увеличивается.
На прогностические данные влияют такие показатели, как уровень аммиака в крови, высокое внутричерепное давление. У детей, перенесших синдром Рея, может сохраняться задержка умственного развития, эпилептические расстройства, судороги, периферическая нейропатия.
| Плохие прогностические признаки |
| Быстрое течение болезни на первых трех клинических стадиях (быстрое развитие сопора и комы) |
| Судороги на третьей стадии |
| Уровень аммиака в крови превышает 300 мгк/мл |
| Повышение внутричерепного давления на третьей стадии |
| Развитие геморрагических осложнений (повышение ПВТ, ПТИ, МНО) |
Ацетилсалициловая кислота и синдром Рея
Ученые предполагают,
что салицилаты нарушают процессы бета-окисления при синдроме Рея.
Предполагаемый механизм таков:
- Вирусы являются пирогенами. Это значит, что, попадая в организм, они продуцируют интерлейкины и факторы некроза опухолей (ФНО). При приеме салицилатов уровень ФНО возрастает в сыворотке крови, что приводит к росту активности воспаления;
- После всасывания ацетилсалициловой кислоты ее метаболизм проходит в митохондриях и клетках печени. Продукты их распада тормозят бета-окисление (окисление пальмитиновой кислоты);
- Высокие концентрации метаболитов салицилатов открывают циклоспоринчувствительные каналы на внутренней мембране митохондрий. Это приводит к гибели органеллы и апоптозу клетки;
- Нарушение окисления жирных кислот и окислительного фосфорилирования приводит к накоплению в клетке жирных кислот (жировая дистрофия).
Печеночная энцефалопатия (возрастные отличия)
Синдром Рея развивается у детей и подростков. Средний возраст заболевших – 4-12 лет. Возникает при лечении лихорадки вирусного происхождения салицилатами. Например, при гриппе, кори, ветрянке.
Острая печеночная энцефалопатия считается заболеванием детского возраста. Однако, описаны несколько зарегистрированных случаев заболевания у взрослых. Были выявлены другие лекарственные средства, которые вызывают сходный по клинике синдром. Это димедрол, ацедипрол, амиодарон, кальция гомопантотенат. А также зафиксированы случаи наследственной ферментопатии и рецидивирующего синдрома Рея у взрослых.
Диагностика
Специалисту с трудом дается диагностика синдрома Рея, так как нет характерной симптоматики, присущей именно этой болезни.
Доктору необходимо:
- провести осмотр больного;
- узнать о наличии хронических заболеваний у пациента;
- выявить жалобы ребенка.
В обязательном порядке назначается прохождение лабораторных исследований:
- общий анализ крови;
- общий анализ мочи;
- биохимический анализ крови;
- тест на нарушение окисления жирных кислот.
Из неинвазивных методов обследования практикуется назначение ультразвуковой диагностики органов брюшной полости.
Возможно предписание инвазивных диагностических процедур:
- люмбальная пункция (для опровержения энцефалита и менингита) — взятие из позвоночника ребенка небольшого количества цереброспинальной жидкости;
- биопсия печени (для исключения иных заболеваний, которые спровоцировали поражение органа) — специалист делает прокол живота в области печени для диагностики;
- биопсия кожного покрова (берется небольшой участок кожи для анализа на нарушение окисления жирных кислот);
- компьютерная и/или магнитно-резонансная томография (возможность увидеть подробное изображение мозга, чтобы было понятно, что стало причиной изменений состояния больного).
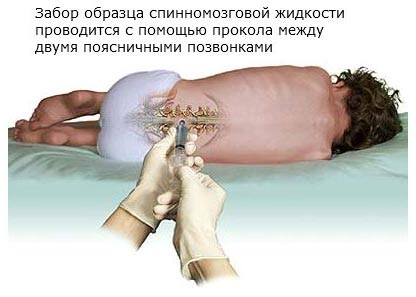 Как делается люмбальная пункция
Как делается люмбальная пункция
Клиницисту необходимо грамотно уметь дифференцировать заболевание от нижеперечисленных:
- сепсис;
- гипертермия (у младенцев до 1 года);
- менингит;
- синдром Шелдона-Рея;
- острый гепатит;
- субарахноидальное кровоизлияние;
- отравление;
- аминоацидурия;
- врожденное нарушение обмена углеводов.
После полного преодоления патологического состояния пациенты должны посетить генетика для получения консультации, основанной на выявлении врожденных заболеваний.