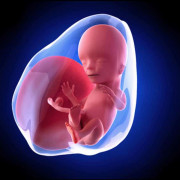
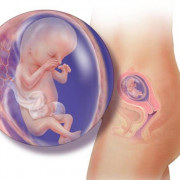
Функции белков в организме
Содержание:
Аминокислоты
Белки состоят из аминокислотной цепи. Аминокислоты связываются между собой с образованием пептидных цепей, более 10 аминокислот — полипептиды.
Общая формула аминокислот H 2 N – CHR – COOH. Строение отдельных аминокислот кардинально отличается. Согласно им выделяют три основные группы аминокислот:
- алифатические;
- ароматические;
- гетероциклические.
Алифатические кислоты делятся на моноаминомонокарбоновые и моноаминодикарбоновые кислоты. В молекуле трех аминокислот — цистеина, цистина и метионина содержится атом серы.
Строение аминокислот
Аминокислоты — бесцветные кристаллические вещества. За исключением глицина, все они имеют асимметричный атом углерода и оптически активны. Человеческий белок содержит 20 отдельных аминокислот. Некоторые из них незаменимы (существенны), другие — заменяемы, потому что их можно синтезировать.
Во время катаболизма всех аминокислот образуются шесть веществ, которые участвуют в общем катаболическом процессе. Эти вещества представляют собой пируват, ацетил-КоА, кетоглутарат, сукцинил-КоА, фумарат и оксалоацетат.
Аминокислоты, из которых промежуточные продукты цикла Кребса (α-кетоглутарат, сукцинил-КоА, фумарат) образуются во время катаболизма и впоследствии превращаются в конечный продукт оксалоацетат и могут использоваться для гликогенеза, называются гликогенными аминокислотами.
Некоторые аминокислоты превращаются в ацетоацетат или ацетил-CoA во время катаболизма и могут использоваться для синтеза ацетоновых материалов. Их называют кетогенными. Многие аминокислоты используются в синтезе веществ глюкозы и ацетона, потому что катаболизм производит два продукта, соответствующий метаболит цикла Кребса и ацетоацетат (Tyr, Phe, Trp) или ацетил-КоА (Ile). Такие аминокислоты называют смешанными или гликокетогенными.
Почти все природные аминокислоты (за исключением метионина) реагируют с α-кетоглутаровой кислотой. Эта катализируемая трансаминазой реакция дает глутаминовую кислоту и соответствующую α-кетоновую кислоту. Образовавшаяся глутаминовая кислота подвергается окислительному дезаминированию под действием каталитической глутаматдегидрогеназы.
Внутриклеточные регуляторные белки
Белки регулируют процессы, происходящие внутри клеток, при помощи нескольких механизмов:
- взаимодействия с молекулами ДНК (транскрипционные факторы);
- при помощи фосфорилирования (протеинкиназы) или дефосфорилирования (протеинфосфатазы) других белков;
- при помощи взаимодействия с рибосомой или молекулами РНК (факторы регуляции трансляции);
- воздействия на процесс удаления интронов (факторы регуляции сплайсинга);
- влияния на скорость распада других белков (убиквитины и др.).
Белки-регуляторы транскрипции
Транскрипционный фактор
— это белок, который, попадая в ядро , регулирует транскрипцию ДНК, то есть считывание информации с ДНК на мРНК (синтез мРНК по матрице ДНК). Некоторые транскрипционные факторы изменяют структуру хроматина, делая его более доступным для РНК-полимераз. Существуют различные вспомогательные транскрипционные факторы, которые создают нужную конформацию ДНК для последующего действия других транскрипционных факторов. Еще одна группа транскрипционных факторов — это те факторы, которые не связываются непосредственно с молекулами ДНК, а объединяются в более сложные комплексы с помощью белок-белковых взаимодействий.
Факторы регуляции трансляции
Трансляция
— синтез полипептидных цепей белков по матрице мРНК, выполняемый рибосомами. Регуляция трансляции может осуществляться несколькими способами, в том числе и с помощью белков-репрессоров, которые, связываются с мРНК. Известно много случаев, когда репрессором является белок, который кодируется этой мРНК. В этом случае происходит регуляция по типу обратной связи (примером этого может служить репрессия синтеза фермента треонил-тРНК-синтетазы).
Факторы регуляции сплайсинга
Внутри генов эукариот есть участки, не кодирующие аминокислот. Эти участки называются интронами . Они сначала переписываются на пре-мРНК при транскрипции, но затем вырезаются особым ферментом. Этот процесс удаления интронов, а затем последующее сшивание концов оставшихся участков называют сплайсингом (сшивание, сращивание). Сплайсинг осуществляется с помощью небольших РНК, обычно связанных с белками, которые называются факторами регуляции сплайсинга. В сплайсинге принимают участие белки, обладающие ферментативной активностью. Они придают пре-мРНК нужную конформацию. Для сборки комплекса (сплайсосомы) необходимо потребление энергии в виде расщепляемых молекул АТФ, поэтому в составе этого комплекса есть белки, обладающие АТФ-азной активностью.
Существует альтернативный сплайсинг . Особенности сплайсинга определяются белками, способными связываться с молекулой РНК в областях интронов или участках на границе экзон-интрон. Эти белки могут препятствовать удалению одних интронов и в то же время способствовать вырезанию других. Направленная регуляция сплайсинга может иметь значительные биологические последствия. Например, у плодовой мушки
Существуют
несколько видов защитных функций белков:
Физическая
защита. В ней принимает участие коллаген —
белок, образующий основу межклеточного
вещества соединительных тканей (в том
числе костей, хряща, сухожилий и глубоких
слоёв кожи (дермы)); кератин,
составляющий основу роговых щитков,
волос, перьев, рогов и др. производныхэпидермиса.
Обычно такие белки рассматривают как
белки со структурной функцией. Примерами
этой группы белков служат фибриногены итромбины ,
участвующие в свёртывании крови.
Химическая
защита. Связывание токсинов белковыми
молекулами может обеспечивать их
детоксикацию. Особенно важную роль в
детоксикации у человека играют ферменты печени,
расщепляющие яды или переводящие их в
растворимую форму, что способствует
их быстрому выведению из организма .
Иммунная
защита. Белки, входящие в состав крови и
других биологических жидкостей,
участвуют в защитном ответе организма
как на повреждение, так и на атаку патогенов.
Белки системы
комплемента и антитела (иммуноглобулины)
относятся к белкам второй группы; они
нейтрализуют бактерии, вирусы или
чужеродные белки. Антитела, входящие
в состав адаптативной
иммунной системы,
присоединяются к чужеродным для данного
организма веществам, антигенам,
и тем самым нейтрализуют их, направляя
к местам уничтожения. Антитела
могутсекретироваться в
межклеточное пространство или
закрепляться в мембранах
специализированных В-лимфоцитов,
которые называютсяплазмоцитами .
В то время как ферменты имеют ограниченное
сродство к субстрату, поскольку слишком
сильное присоединение к субстрату
может мешать протеканию катализируемой
реакции, стойкость присоединения
антител к антигену ничем не ограничена .
Основные функции белков
Функции белков в организме многообразны. Каждая группа имеет определенное химическое строение, совершает одну специализированную «работу». В некоторых случаях несколько типов белков взаимосвязаны друг с другом. Они отвечают за разные этапы одного процесса. Или же влияют сразу на несколько. Например, регуляторная функция белков осуществляется ферментами и гормонами. Это явление можно представить, вспомнив о гормоне адреналине. Он вырабатывается мозговым слоем надпочечников. Поступая в кровеносные сосуды, он повышает количество кислорода в крови. Поднимается и артериальное давление, увеличивается содержание сахара. Это стимулирует обменные процессы. Также адреналин является медиатором нервной системы у рыб, амфибий и пресмыкающихся.
Коллаген
Коллаген — это основной белок соединительной ткани у животных. Коллаген содержится в костях, хрящах, сухожилиях, зубах, коже, роговице, легких, печени, кровеносных сосудах и других органах и тканях. На его долю приходится около 25-30% белка млекопитающих.
У человека и позвоночных было идентифицировано двенадцать типов коллагена, состоящего из более чем 24 различных полипептидных α-спиралей. Комбинации этих спиралей определяют типы коллагена. Например, наиболее распространенный коллаген I типа (90% общей массы коллагена) состоит из 2 спиралей α-1 и 1 α-2.
Структура коллагена
Коллаген отличается от других белков организма своим уникальным аминокислотным составом: 33%. из всех аминокислот составляют Gly, 10% – про, 10% – гидрокси-Pro и 1% – гидрокси-Lys. Основная структурная единица коллагена — тропоколаген, состоит из трех левовращающихся α-спиралей, скрученных в одну правовращающуюся суперспираль. Такие суперспирали связываются поперечными ковалентными связями с образованием фибрилл.
Бизнес и финансы
БанкиБогатство и благосостояниеКоррупция(Преступность)МаркетингМенеджментИнвестицииЦенные бумагиУправлениеОткрытые акционерные обществаПроектыДокументыЦенные бумаги — контрольЦенные бумаги — оценкиОблигацииДолгиВалютаНедвижимость(Аренда)ПрофессииРаботаТорговляУслугиФинансыСтрахованиеБюджетФинансовые услугиКредитыКомпанииГосударственные предприятияЭкономикаМакроэкономикаМикроэкономикаНалогиАудитМеталлургияНефтьСельское хозяйствоЭнергетикаАрхитектураИнтерьерПолы и перекрытияПроцесс строительстваСтроительные материалыТеплоизоляцияЭкстерьерОрганизация и управление производством
3. Внутриклеточные регуляторные белки
Белки регулируют процессы, происходящие внутри клеток, при помощи нескольких механизмов:
- взаимодействия с молекулами ДНК (транскрипционные факторы)
- при помощи фосфорилирования (протеинкиназы) или дефосфорилирования (протеинфосфатазы) других белков
- при помощи взаимодействия с рибосомой или молекулами РНК (факторы регуляции трансляции)
- воздействия на процесс удаления интронов (факторы регуляции сплайсинга)
- влияния на скорость распада других белков (убиквитины и др.)
3.1. Белки-регуляторы транскрипции
Транскрипционный фактор
— это белок, который, попадая в ядро, регулирует транскрипцию ДНК, то есть считывание информации с ДНК на мРНК (синтез мРНК по матрице ДНК). Некоторые транскрипционные факторы изменяют структуру хроматина, делая его более доступным для РНК-полимераз. Существуют различные вспомогательные транскрипционные факторы, которые создают нужную конформацию ДНК для последующего действия других транскрипционных факторов. Еще одна группа транскрипционных факторов — это те факторы, которые не связываются непосредственно с молекулами ДНК, а объединяются в более сложные комплексы с помощью белок-белковых взаимодействий.
3.2. Факторы регуляции трансляции
Трансляция
— синтез полипептидных цепей белков по матрице мРНК, выполняемый рибосомами. Регуляция трансляции может осуществляться несколькими способами, в том числе и с помощью белков-репрессоров, которые, связываются с мРНК. Известно много случаев, когда репрессором является белок, который кодируется этой мРНК. В этом случае происходит регуляция по типу обратной связи (примером этого может служить репрессия синтеза фермента треонил-тРНК-синтетазы).
3.3. Факторы регуляции сплайсинга
Внутри генов эукариот есть участки, не кодирующие аминокислот. Эти участки называются интронами. Они сначала переписываются на пре-мРНК при транскрипции, но затем вырезаются особым ферментом. Этот процесс удаления интронов, а затем последующее сшивание концов оставшихся участков называют сплайсингом (сшивание, сращивание). Сплайсинг осуществляется с помощью небольших РНК, обычно связанных с белками, которые называются факторами регуляции сплайсинга. В сплайсинге принимают участие белки, обладающие ферментативной активностью. Они придают пре-мРНК нужную конформацию. Для сборки комплекса(сплайсосомы) необходимо потребление энергии в виде расщепляемых молекул АТФ, поэтому в составе этого комплекса есть белки, обладающие АТФ-азной активностью.
Существует альтернативный сплайсинг. Особенности сплайсинга определяются белками, способными связываться с молекулой РНК в областях интронов или участках на границе экзон-интрон. Эти белки могут препятствовать удалению одних интронов и в то же время способствовать вырезанию других. Направленная регуляция сплайсинга может иметь значительные биологические последствия. Например, у плодовой мушки дрозофилы альтернативный сплайсинг лежит в основе механизма определения пола.
3.4. Протеинкиназы и протеинфосфатазы
Важнейшую роль в регуляции внутриклеточных процессов играют протеинкиназы — ферменты, которые активируют или подавляют активность других белков путем присоединения к ним фосфатных групп.
Протеинкиназы регулируют активность других белков путем фосфолирования — присоединения остатков фосфорной кислоты к остаткам аминокислот, имеющих гидроксильные группы. При фосфорилировании обычно изменяется функционирование данного белка, например, ферментативная активность, а также положение белка в клетке.
Существуют также протеинфосфатазы — белки,которые отщепляют фосфатные группы. Протеинкиназы и протеинфосфатазы регулируют обмен веществ, а также передачу сигналов внутри клетки. Фосфорилирование и дефосфорилирования белков — один из главным механизмов регуляции большинства внутриклеточных процессов.
Цикл активации G-белка под действием рецептора.
Синхронизация выполнена 18.07.11 07:59:14
Что такое белок и каковы его функции
На уроках биологии и химии довольно много времени уделяется этой важной теме. Белки (protein) являются природными гетерополимерами, состоящие из α-аминокислот
Соединяет их вместе пептидная связь. Для синтеза огромного множества белков в человеческом организме используется 20.

Состав каждого белка, синтезированного в организме, определяется геномом. Различные комбинации генетического кода позволяют создавать из стандартных аминокислот огромное множество белков, отвечающих за разнообразные функции в нашем теле.
Некоторые белки довольно сложно классифицировать исключительно по их функциям. Так как один белок часто может отвечать за выполнение нескольких задач.

Список функций белков выглядит следующим образом:
- Структурная – отвечает за образование цитоскелета клеток, придает форму разным тканям. Наиболее известные это коллагены и эластин, входящие в состав межклеточного вещества. А также кератин – основной белок, формирующий ногти и волосы.
- Защитная функция разделяется на физическую, иммунную и химическую. За физическую защиту в основном отвечают тромбины, свертывающие кровь, и коллагены и кератин, формирующие роговые щитки, волосы, кожу. Химическую защиту от различных токсинов в организме выполняют в основном ферменты печени. Они растворяют токсины, позволяя быстрее вывести их. За иммунную защиту отвечают различные иммуноглобулины.
- Каталитическая функция использует ферменты. Это особые белки, позволяющие катализировать реакции, расщепляющие большие молекулы, или же наоборот их синтезировать. Ферменты позволяют ускорять все химические реакции в сотни и тысячи раз. За последнее время науке стало известно свыше 5000 различных ферментов.
- Регуляторная функция отвечает за управление всей жизнедеятельностью клетки. Белки из данной группы регулируют количество и активность остальных белков, а также множество процессов внутри самой клетки.
- Сигнальная функция выполняется гормонами и цитокинами. Эти белки являются сигнальным веществом, позволяя передавать информацию или сигналы частями организма.
- Транспортная – позволяет переносить различные вещества от одних органов и клеток к другим. Наиболее известный пример – это гемоглобин, транспортирующий кислород и углекислый газ.
- Запасная функция. Ее выполняют белки, запасающиеся в организме для экстренных случаев в качестве энергии или источника аминокислот.
- Рецепторная. Ее выполняют белки, реагирующие свет, физическое воздействие или химическое вещество.
- Моторная функция выполняется целыми группами белков. Среди них, например, актин и миозин. Они являются основными компонентами мышц и позволяют им сокращаться. Другие белки позволяют клеткам лейкоцитов передвигаться внутри организма.
Роль РНК и ДНК в процессе
Итак, запускает синтез белков в клетках цепочка ДНК, которая несет информацию о каком-либо конкретном белке и называется геном. Цепочка ДНК в процессе транскрипции расплетается, то есть её спираль начинает распадаться в линейную молекулу. С ДНК информация должна преобразоваться на РНК. Напротив тимина в данном процессе должен становиться аденин. Цитозин же имеет в качестве пары гуанин, точно так же, как ДНК. Напротив аденина РНК становится урацил, потому как в РНК такого нуклеотида, как тимин, не существует, он заменяется просто урациловым нуклеотидом. С гуанином соседствует цитозин. Напротив аденина становится урацил, а в паре с тимином располагается аденин. Эти молекулы РНК, которые становятся напротив, называются информационными РНК (иРНК). Они способны через поры выходить из ядра в цитоплазму и рибосомы, которые, собственно, и выполняют функцию синтеза белков в клетках.
Функции белков в клетке
- Строительная (пластическая) функция белковых молекул является одной из важнейших.Они являются составным компонентом клеточных мембран и органел. Стенки кровеносных сосудов, сухожилия, хрящи высших животных также состоят в основном из белка.
- Двигательная функция обеспечивается особенными сократительными белками, благодаря которым осуществляются движения жгутиков и ресничек, перемещение хромосом во время деления клеток, сокращение мускулатуры, движения органов растений и т.п., пространственные изменения положения различных структур организма.
- Транспортная функция белков обеспечивается их способностью связывать и переносить с течением крови химические соединения.
Пример 2
Белок крови гемоглобин переносит кислород из лёгких в клетки других органов и тканей (аналогичную функцию в мышцах выполняет миоглобин).
Белки сыворотки крови переносят липиды и жирные кислоты, различные биологически активные вещества.
Молекулы белков, входящих в состав плазматической мембраны, берут участие в транспорте веществ как в клетку, так и из неё.
Белки выполняют и защитную функцию. Как ответ на проникновение внутрь чужеродных веществ (антигенов – белков или высокомолекулярных полисахаридов бактерий, вирусов) в клетке вырабатываются особенные белки – иммуноглобулины (антитела), которые нейтрализуют чужеродные вещества и осуществляют иммунологичную защиту организма.
Благодаря функционированию иммунной системы организма обеспечивается распознавание антигенов антигенным детерминантам (характерным участкам их молекул). Благодаря этому специфически связываются и обеззараживаются чужеродные вещества за.
Замечание 5
Внешнюю защитную функцию могут выполнять также и белки, токсические для других организмов ( белок яда змей).
Белкам свойственна также сигнальная функция. В поверхность клеточной мембранны встроены молекулы белков, которые в ответ на действия факторов внешней среды способны к изменению свей третичной структуры. Так происходит восприятие сигналов из внешней среды и передача команд в клетку.
Регуляторная функция свойственна белкам-гормонам, которые влияют на обмен веществ. Гормоны поддерживают постоянную концентрацию веществ в крови, учавствуют в росте размножении и других жизненно важных процессах.
Пример 3
Одним из наиболее известных гормонов является инсулин, понижающий содержание сахара в крови. В случае стойкой недостаточности инсулина содержание сахара в крови увеличивается и развивается сахарны диабет. Главными регуляторами биохимических процессов в организме могут быть и многочисленные белки-ферменты (каталитическая функция).
Белки являются и энергетическим материалом. При расщеплении 1 г белка до конечных продуктов выделяется 17,6 кДж энергии, необходимой для большинства жизненно важных процессов в клетке.
Что такое белки
Белки представляют собой органические соединения, имеющие различный состав и выполняющие важные функции в организме всех живых существ. Существует несколько видов этих молекул, каждый из которых имеет значение в процессе жизнедеятельности.
Состав
Органические вещества являются высокомолекулярными, поэтому могут включать в свой состав различные аминокислоты и другие соединения. Набор важных компонентов в каждой молекуле закладывается генетическим кодом животного или человека.
Основные компоненты каждой молекулы:
- углерод;
- кислород;
- азот;
- водород;
- сера.
Первый компонент обнаруживается в белке в наибольшем количестве, последний — не более 5 % от состава.

История открытия
Первый белок был получен необычным способом. Его выделили из пшеничной муки в виде клейковины. Произошло открытие в 1728 году, сделал его Якопо Беккари, итальянец. В качестве отдельного биологического класса молекулы белка были выделены в XVIII веке после обнародования работ французского ученого и химика Антуана де Фуркруа.
Другие ученые одновременно с французом отметили, что молекулы имеют свойство коагулировать (объединяться) под воздействием некоторых кислот или в процессе нагревания.
На тот момент ученые смогли изучить только альбумин, фибрин и глютен.
Только через 100 лет, в XIX веке, другие исследователи, изучив состав простых белков, отметили, что при нагревании происходит выделение аминокислот. Это помогло сделать вывод, что молекулы включают в себя довольно большое количество важных и разных аминокислот, а состав каждой из них индивидуален.
В 1836 году Мульдер предложил первую структурную формулу белков, основанную на теории радикалов. Он и еще несколько ученых вывели формулу протеинов, что в переводе с греческого означает «первый». Мульдер также определил почти точную молекулярную массу наиболее простого белка, равную 131 дальтону. Дальтон — единица измерения молекул, называемая еще атомной массой или углеродной единицей.
Позже ученые выявили, что молекулярная масса может быть различной и зависит от состава и структуры органического соединения.
В 1880-х годах русский ученый Данилевский изучил пептидные группы и доказал их существование в белковой молекуле. К этому времени большинство аминокислот уже были изучены.
В 1894 году немецкий ученый и физиолог Альбрехт Коссель рассказал о своем предположении. Он считал, что именно аминокислоты являются основными структурными элементами белковой молекулы. Его теория была подтверждена в начале ХХ века химиком из Германии Эмилем Фишером. Ученый в ходе своего эксперимента доказал, что каждая молекула содержит около 20 аминокислот.
Важность белка в живом организме была признана только в 1926 году благодаря эксперименту американца Джеймса Самнера. После этого начинается активное изучение структур молекулы, выделяются различные виды
В 60—80-ых годах ХХ века исследования продолжаются.
К 2012 году в базе данных насчитывалось около 87 тысяч структур.
Сегодня методы изучения молекулы усовершенствованы, поэтому работа в этом направлении продолжается.

Строение
Белок считается макромолекулой, поскольку имеет большой размер и множество составляющих. В строении белков присутствуют разные аминокислоты или их остатки, они чередуются с полипептидными цепями.
В молекулу могут входить следующие аминокислоты:
- глицин;
- аланин;
- изолейцин;
- серин;
- лейцин;
- валин;
- треонин.
Эти встречаются в составе наиболее часто, сочетаются с пептидными цепями и аминокислотными остатками.

Активная защитная функция
Белковые яды животных
Белки могут служить также для защиты от хищников или нападения на добычу. Такие белки и пептиды содержатся в ядах большинства животных (например, змей, скорпионов, стрекающих и др.). Содержащиеся в ядах белки имеют различные механизмы действия. Так, яды гадюковых змей часто содержат фермент фосфолипазу, который вызывает разрушение клеточных мембран и, как следствие, гемолиз эритроцитов и геморрагию. В яде аспидов преобладают нейротоксины; например, в яде крайтов содержатся белки α-бунгаротоксин (блокатор никотиновых рецепторов ацетилхолина и β-бунгаротоксин(вызывает постоянное выделение ацетилхолина из нервных окончаний и тем самым истощение его запасов); совместное действие этих ядов вызывает смерть от паралича мышц.
Бактериальные белковые яды
Бактериальные белковые яды — ботулотоксин, токсин тетаноспазмин, вырабатываемый возбудителями столбняка, дифтерийный токсин возбудителя дифтерии, холерный токсин. Многие из них являются смесью нескольких белков с разным механизмом действия. Некоторые бактериальные токсины белковой природы являются очень сильными ядами; компоненты ботулотоксина — наиболее ядовитое из известных природных веществ.
Токсины патогенных бактерий рода Clostridium, видимо, требуются анаэробным бактериям для воздействия на весь организм в целом, чтобы привести его к смерти — это дает бактериям «безнаказанно» питаться и размножаться, а уже сильно увеличив свою популяцию покидать организм в виде спор.
Биологическое значение токсинов многих других бактерий точно не известно.
Белковые яды растений
У растений в качестве ядов обычно используются вещества небелковой природы (алкалоиды, гликозиды и др.). Однако у растений встречаются и белковые токсины. Так, в семенах клещевины (растения семейства молочайные) содержится белковый токсин рицин. Этот токсин проникает в цитоплазму клеток кишечника, и его ферментативная субъединица, воздействуя на рибосомы, необратимо блокирует трансляцию.